1
解答 解答用紙 指定さ 箇所 記入 。
必要 あ 次 数値 用い 。
原子量:H = 1.0 C = 12 N = 14 O = 16 Na = 23 Cl = 35.5
定数:6.02 × 10
23 / mol 気体定数:8.3 × 10
3
Pa·L / (K· mol)
定数:9.65 × 10
4
C / mol
ウ 温度目盛 点 0 °C:273 K
2
問 次 ~ 問い い 正 い 〜 う
1 選び 番号 答え 。 点
次 イ ン う イ ン半径 最 大 い 。
Na+ Mg2+ Al3+ F O2
次 水素化合物 う 常 沸点 最 高い 。
NH3 H2O H2S HBr CH4
次 操作 う 水 置換 捕集 気体 発生 。
塩化 ウ 濃硫酸 加え 熱 。
銅 濃硝酸 加え 。
銅 濃硫酸 加え 熱 。
亜鉛 希硫酸 加え 。
3
次 元素 う 黄色 炎色 応 示 。
Li Na K Ca Cu
次 う 応熱 応 経路 応 初 状態 終わ
状態 決 いう法則 。
法則
法則
ン ッ 法則
ン 法則
イ 法則
次 酸化物 う 塩基性酸化物 。
4
次 芳香族化合物 う 解熱鎮痛薬 用い 。
次 糖 う 二糖類 水溶液 還元性 示 。
コ
5
6
次 記述 読 問い 問 ~問 答え 。 点
1869 化学者 ン エ 当時知 い 約60種類 元
素 原子量 順 並 性質 く似 元素 周期的 出現 規則性 発見
周期表 発表 。現 周期表 元素 原子量 く原子番号 順
並 あ 。周期表 横 行 [ A ] いい 順 第1[ A ],
第2[ A ] 呼 。一方 縦 列 [ B ] いい 順 1[ B ],
2[ B ] 呼 。
図 周期表 う 第4[ A ] 示 あ 。長方形 1
1 元素 示 。斜線 付け 元素 [ ]元素 いい 金属元素
あ 。[ ]元素 一 [ A ] い 隣 合う元素 う 性質
似 い 場合 多い。こ 原子 [ イ ] 数 [ ウ ] [ エ ]
ほ 変化 い あ 。 Sc Cu 電子殻 う [ ]殻
電子 増加 Cu [ ]殻 容可能 最大数 あ [ ]個 電子
入 い 。
[ ]元素以外 元素 [ ]元素 呼 金属元素 非金属元素 約
半数 含 。 [ B ] [ ]元素 数 [ ] 持 互い
く似 化学的性質 示 。 え 図 印 元素 単体 水 容易
応 気体 発生 強い[ ]性 示 水酸化物 生 。 印 元素 化
合物 く くく 単体 単原子 子 。 原子
H
◆
☆
◆ #
◆ ◆ #
Sc Cu #
第1 A
第2 A
第3 A
第4 A
7
[ イ ] 数 [ コ ] 8 あ [ ] 数 0 。#印 元
素 単体 い [ サ ]作用 示 [ サ ] 力
く
原子番号 大 く
ほ [ ]く 。 #印 3 元素 う 原子番号 2番
目 大 い (X 表 ) 単体 X2 原子番号 最 大 い (Z 表 )
ウ 塩 KZ 次 う 応 。
2 KZ X2 → 2 KX Z2
問 文中 [ A ][ B ][ ]~[ ] 適 語句 数 記
入 。
問 Be Br K Mn P Si 元素 う 金属元素 ○ 非金属元素
× 解答欄 記入 。
問 図 印 印 び #印 元素 固有 称 呼 元
8
問 次 〜 (縦軸 単 省略さ い ) う 元素
原子番号 イ ン化エ (第一イ ン化エ ) 関係 表
い 。1 選 。
0 0.250
原子番号
原子番号
原子番号
原子番号 0.200 0.150 0.100 0 0.050 3000 2000 1000 0 7 6 5 4 3 2 1 0 2500 2000 1500 1000 500 10 10
10 20 30 40
20 30 40
20 30 40
9
問 図 ◆印 元素 い い 性質 異 複数 単体
。こ 関係 表 適 語句 解答欄 記入 。 ◆印 元素
う 最 原子番号 小さい元素 い 具体例 性質 異
単体 称 2 答え 。
問 図 ☆印 元素 原子 原子核 不安定 放射線 放出 自然
別 原子核 変わ 体 。こ 体 例 線部
元素記号 用い 表 。
例:水素H 構成 体 う H
1
1 比 99.9% 以 あ 。
問 線部 応 い 図 印 3 元素 う 原子番号 2番目
大 い元素 例 化学 応式 記 。
10
次 記述 読 問い 問 ~問 答え 。 点
図 示 ン 備え 密閉容器 用い 以 実験 行 。
実験 こ 容器内 水H2O 0.400 mol 窒素N2 0.500 mol 入 ン
抵抗 く自由 移動 状態 容器全体 27 °C 保 衡
放置 。
実験 実験 状態 ン 置 固定 後 容器全体 温度
87 °C 。
窒素 び水蒸気 理想気体 い 容器内 水 体積 び水
窒素 子 溶解 ン び容器自体 熱 変形 無視
。 27 °C け 飽和水蒸気 4.00 × 10
3
Pa 87 °C け 飽和水蒸
気 6.00 × 10
4
Pa 。 大気 1.04 × 10
5
Pa 。
問 実験 状態 け 容器内 気体 体積 L いく 。有効数 3
桁 答え 。
H2O 0.400 mol
N2 0.500 mol
ピ ス ト ン 左方向へ移動
11
問 実験 状態 い 容器内 液体 水 物質量 mol
いく 。有効数 3桁 答え 。
問 実験 状態 い 容器内 気体 示 力 Pa いく 。有効
数 3桁 答え 。
12
問 実験 状態 ン 移動さ こ 水蒸気 1.50 × 10
4
Pa 。こ 容器内 気体 体積 L いく 。有効数 3
桁 答え 。 容器全体 温度 87 °C 一定 。
13
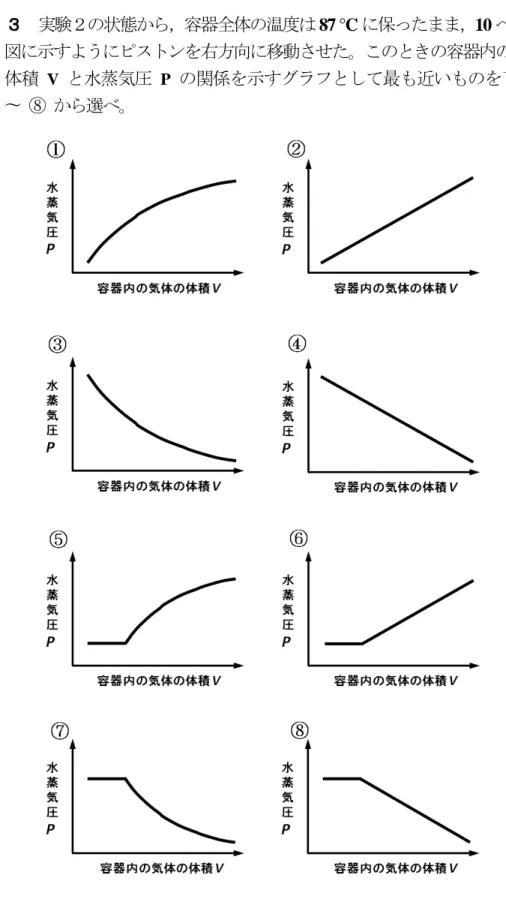
問 実験 状態 容器全体 温度 87 °C 保 10
図 示 う ン 右方向 移動さ 。こ 容器内 気体
体積 V 水蒸気 P 関係 示 最 近い
14
次 記述 読 問い 問 〜 答え 。 点
ン NH3 常温 常 無色 刺激臭 あ 気体 あ 業的
鉄 酸化物 触媒 用い 窒素 N2 水素 H2 直接 合成 。こ
NH3 製法 [ ]法 いう。
NH3 弱塩基 あ 水 溶 一部 け 電離 生 イ ン
NH4+ 電離 い い 子 間 次 う 電離 衡 成立 。
NH3 H2O NH4+ + OH−
式 電離 衡 衡定数K 衡状態 け NH3 NH4
+
濃度 mol/L あ [ NH3 ] [ NH4
+
] 用い 式 う 表さ
。
K =
ここ H2O 濃度 一定 こ ン 塩基 電離定
数 Kb 式 う 表さ 。
Kb =
NH4+ [ イ ]イ ン 呼 陽イ ン あ NH3 子 [ ウ ]
電子対 水素イ ン 提供 こ 生成 。ここ 結合 特
[ エ ]結合 いう 普通 共有結合 区別 い。こ NH3 子
角錐形 あ 対 NH4
+
[ ]形 あ 。
NH4 +
塩化物 あ NH4Cl 水溶液中 式 う 電離 生
NH4+ 式 う [ ] 子 応 [ ] 子 生成 。
結果 [ ]イ ン 濃度 大 く 水溶液 弱酸性 。こ う
現象 塩 [ ] いう。
NH4Cl NH4+ + Cl−
15
25 °C い 0.10 mol/L NH3 水溶液 10 mL コ 取 0.025
mol/L 塩酸 滴定 こ 中和点 [ ]mL 要 。中和点
コ内 溶液 [ ]mol/L NH4Cl 水溶液 い 。
問 [ ]〜[ ] 入 適 語句 数値 記 。数値 有効数
2桁 答え 。
問 式 適 式 記 。
16
問 線部 滴定 い 次 (a) ~ (c) 水溶液 pH いく 。小
数点第1 求 。 25 °C け NH3 Kb 2.0 10
−5 mol/L
,水のイオン積Kw = 1.0 10 −14
(mol/L)2 。必要な ばlog102 = 0.30,
log103 = 0.48 の値を用い 。
(a) 滴定開始前 水溶液 0.10 mol/L NH3 水溶液
(b) 中和点の水溶液
式 け 辺 右辺 応 進行 極 わ
あ 。
(c) [ ] 半 体積 mL 0.025 mol/L 塩酸 滴 水
溶液
17
18
塩化 ウ 関 次 問い 問 ~問 答え 。
点
問 次 〜 う 塩化 ウ 結晶構造 正 い
。1 選 。 ○ Na ● Cl 示 。
問 1 mol 塩化 ウ 結晶中 結合 断 気体状態
イ ン 必要 エ 塩化 ウ 格子エ
いう。格子エ Q kJ/mol 次 熱化学方程式 表
こ 。
NaCl(固) = Na (気) Cl (気) Q kJ
塩化 ウ 格子エ Q kJ/mol いく 。整数 答え 。
以 熱化学方程式 成立 。
Na(固) Cl2(気) = NaCl(固) 411 kJ Na(固) = Na(気) 92 kJ
Na(気) = Na (気) e 496 kJ Cl2(気) = 2 Cl(気) 244 kJ
Cl(気) e = Cl (気) 349 kJ
2
19
問 図 う 陽イ ン交換膜 陽極側 陰極側 隔 陽極側
塩化 ウ 飽和水溶液 陰極側 水 入 電気 解 行 。
一定時間後 陰極側 水酸化 ウ 水溶液(水溶液X )1.00 L
得 。こ 水溶液X全量 0.100 mol/L 硫酸水溶液 中和 こ
20.0 mL 要 。こ 水溶液X中 水酸化 ウ 生成 流
電気量 C いく 。有効数 3桁 答え 。 流 電流
電気 解 使用さ 。
問 問 電気 解 い 陽極 陰極 発生 気体(気
体A 気体B) 何 。化学式 答え 。 水溶液X 水酸化 ウ
生成 発生 気体 標準状態 け 体積 mL
いく 。有効数 3桁 答え 。 発生 気体 水溶液 溶
解 考え い 。
塩化ナトリウムの 飽和水溶液
気体A 気体B
水
陽イオン交換膜
陽極 (炭素)
陰極
20
次 記述 読 問い 問 〜問 答え 。 構造式
書く場合 例 書け。 点
構造式 例
化合物A B C 子量200以 化合物 い ン ン環 1
エ 結合 1 不斉炭素原子 1 。化合物A B C 元
素 析 行 こ い 質量 率 炭素74.1% 水素7.9%
酸素18.0% あ 。
化合物A 水酸化 ウ 水溶液 加水 解 後 酸 加え 酸性
化合物D E 生成 。化合物B C 様 操作 加水 解
化合物B 化合物F G 生成 化合物C 化合物H
I 生成 。
化合物D 適 触媒 用い エン 空気 酸化 得 化合物
一 あ 。
化合物E 二 酸 ウ 希硫酸水溶液 加え 応さ 中性
化合物J 生成 。
化合物F 濃硫酸 加え 加熱 子内脱水 こ チ ン 生
。
化合物H 適 触媒 用い ン 酸素 酸化 後 硫酸 解
得 化合物 一 あ 。
21
問 化合物A B びI 構造式 書け。
問 化合物D E びH 称 書け。
問 化合物F 構造異性体 う ン ン環 化合物 金属
ウ 小片 加え 水素 発生 い 何種類 。
光学異性体 場合 2 数え 。
問 化合物D〜J う 次 記述 あ 化合物 。該当
記号 答え 。
(a) 不斉炭素原子 。
(b) ウ素 水酸化 ウ 水溶液 加え 温 黄色沈殿 生 。
22
次 記述 読 問い 問 ~問 答え 。 点
あ 天然 タンパ 質 水溶液 濃硝酸 加え 熱 黄色
さ ン 水 加え 塩基性 橙黄色 。こ こ
こ タンパ 質 構成 酸 [ ] う 子内
[ ] 酸 含 い こ わ 。
こ タンパ 質 水溶液 水酸化 ウ 加え 熱 酢酸 中和後
酢酸鉛(II) 加え 黒色沈殿 生 。こ こ こ タンパ 質
構成 酸 [ イ ] う 子内 [ ]原子
酸 含 い こ わ 。
こ タンパ 質 加水 解 こ 鎖状 チ A 得 。こ
チ A さ 加水 解 こ 構造 異 2種類 チ
B C 得 。
チ A B C 水溶液 水酸化 ウ 水溶液 加え
塩基性 後 少量 硫酸銅(II)水溶液 加え A 水溶液 赤
紫色 。
チ A 子式 C13H17N3O5 あ 。
チ A B C い い 線部( ) 応 進行 認
。
問 文中 [ ] [ イ ] あ 酸 次 示
10種類 酸 1 選び 称 記入 。 [ ][ ]
適 語句 記入 。
23
問 構造式 例 チ Aの構造式を書け。 し,ペプチドA
示 10種類 酸 う いく 構成さ い 。
構造式 例
酸 構造式
24
問 次 (a) ~ (d) の記述 最 関連 深い語句 記 (あ) ~ (さ) の選択肢 1 選び 記号 答え 。
(a) 水溶液中 タンパ 質 チ 鎖 - ッ 構造や
-構造 く こ 多い。
(b) 水溶液中 タンパ 質 ン う 膜 通過 い性質 利
用 タンパ 質 子化合物 離 。
(c) 加熱 強酸 強塩基 作用さ タンパ 質 凝固
沈殿 。
(d) タンパ 質 水溶液 大量 硫酸 ウ 加え 沈殿 生 。
選択肢 (あ) 異化 (い) 加水 解 (う) 変性 (え) 透析 ( ) 塩析 ( ) 凝析 ( ) 凝縮
(く) (タンパ 質 ) 一次構造
(け) (タンパ 質 ) 二次構造
(こ) (タンパ 質 ) 次構造
(さ) (タンパ 質 ) 四次構造